日本のバイオベンチャー企業の「ラクオリア創薬」が創出した「Tegoprazan(テゴプラザン)」が、米国での臨床試験(治験)の第III相試験(フェーズ3)を成功裏に完了しました。
しかも、既存薬と比較して優れた効果を示すデータが得られ、逆流性食道炎などの胃食道逆流症(GERD)の治療薬において、「ベスト・イン・クラス(Best-in-Class)」の薬となることが期待されます。
(ベスト・イン・クラスとは、同一カテゴリーの薬の中で、効果や安全性など臨床的な重要性の観点で最も優れる医薬品のこと)
つまり、ただ臨床試験を成功させただけでなく、大成功と言って良いほどの素晴らしい薬を生み出したと言え、逆流性食道炎などの症状がある多くの患者を救うことが期待されます。
そして、このテゴプラザンが、近年の日本バイオベンチャー企業発の医薬品としては異例の
「ブロックバスター」
となる可能性を秘めています。
近年では日本のバイオベンチャー企業が創出した薬で、ブロックバスターになった薬がないと言われているため、テゴプラザンがそれを実現すれば、“歴史的快挙”と言えるでしょう。
一般的には、「ブロックバスター」は、年間1000億円以上の売上をあげる薬のことを指します。
既に、テゴプラザンは、韓国で「K-CAB」という名前で販売されており、韓国だけで年間約200億円売り上げている薬となっています。
元々、韓国のGERDの市場は、そこまで大きくないと推測されていたため、年間約200億円も売れることは、当初は誰も予想していなかったと思われます。
また、中国でも販売され始め、売上が急激に伸びてきている所です。
他の国々でも販売され始めているため、大きな市場の米国、欧州、日本を除いた他の国だけでも、いずれ売上が1000億円を突破する勢いです。
そのため、米国で販売され、順調に売れたら、全世界で年間1000億円を突破する可能性が大きいと予想できます。
現に、ラクオリアは、テゴプラザンを韓国企業の「HKイノエン(HK inno.N)」に導出していますが、そのHKイノエンが、2025年6月の韓国の記事で、2030年に売上3兆ウォン(約3000億円)を目標と述べています。
“케이캡 연 매출, 3조원 달성한다…비만·아토피 약도 출격”
そのため、順調に行けば、ブロックバスターになる確率は高いと考えられます。
Tegoprazan(テゴプラザン)とは
Tegoprazanは、カタカナで「テゴプラザン」と呼びます。
テゴプラザンの説明をラクオリアの公式Webページから引用します。
Tegoprazanは、当社が創出したカリウムイオン競合型アシッドブロッカー(Potassium Competitive Acid Blocker:P-CAB)と呼ばれる新しい作用機序の胃酸分泌抑制剤です。
P-CABは、胃食道逆流症治療の第一選択薬であるプロトンポンプ阻害剤(PPI)とは異なるメカニズムで、PPIよりも速やかに、かつ、持続的に胃酸分泌を抑制するという特長を持つ新世代の治療薬です。
テゴプラザンは、主に「胃食道逆流症(GERD)」の治療薬です。
ちなみに、GERD以外の治療にも使われ、例えば、「胃潰瘍」や「十二指腸潰瘍」の治療、「ヘリコバクター・ピロリ除菌療法」などにも用いられます。
過去には「PPI」というメカニズムの薬が主流でしたが、それよりも、素早く効き、効果的と言われている「P-CAB」という新しいメカニズムのものになります。
ちなみに、2025年8月に市販で発売された「タケプロンS」は、PPIです(それまでは、タケプロンは病院で処方しないと手に入りませんでしたが、ドラッグストアなどで買えるようになりました)。
P-CABでは、日本で武田薬品が販売している「タケキャブ(Vonoprazan、ボノプラザン)」が有名です。
タケキャブは、日本だけで年間約1000億円売れています。
タケキャブは、米国では、「Phathom Pharmaceuticals」という米国企業が開発・販売をしており、「VOQUEZNA」という名前で売られています。
テゴプラザンとタケキャブの差は、色々ありますが、大きな差の1つとしては、タケキャブは、服用してから効果が出るまでに数時間掛かりますが、テゴプラザンは、30分以内~1時間以内で効果が出ます。
その効果が出る速さから、中国などでは、「30分」と強調して販売マーケティングされていたりします。
胃食道逆流症(GERD)とは
胃食道逆流症は、「GERD」とも呼ばれます。
その名前の通り、胃酸などの胃の内容物が食道内へ逆流して起こる病気の総称です。
GERDは、以下の2種類に分類されます。
- びらん性胃食道逆流症(EE: Erosive Esophagitis) ≒ 逆流性食道炎
- 食道粘膜にびらん(ただれ)がある
- 非びらん性胃食道逆流症(NERD: Non-Erosive Reflux Disease)
- 食道粘膜にびらん(ただれ)がない
一般人に馴染み深い名前が「逆流性食道炎」です。
芸能人や有名人もよくこの症状に悩まされており、話題になることがあります。
「びらん性胃食道逆流症」のことを「逆流性食道炎」と扱っていることが多いため、テゴプラザンは、逆流性食道炎の治療薬と思うとわかりやすいと思います。
上記で、「びらん性胃食道逆流症」と「逆流性食道炎」を「=」ではなく「≒」と記載した理由は、厳密に定義分けしている人がいるかもしれないからです。
ただし、ネットで検索した限り、「びらん性胃食道逆流症 = 逆流性食道炎」と扱っている医療記事や医師が書いた記事ばかりなので、一般的には同じ扱いで良いと思われます。
本記事では、以降では、わかりやすいように「逆流性食道炎」と記載します。
逆流性食道炎は、「LA分類(ロサンゼルス分類)」というもので、重症度をグレードで分けています。
内視鏡検査で確認された食道粘膜の損傷があるものにおいて、「A~D」の4段階のグレードに分けられています(「N:正常、M:色調変化のみ」のグレードもあり)。
「A⇒B⇒C⇒D」の順に重症度が増します。
一般的に、「A、Bは軽症」、「C、Dは重症」とみなされます。
逆流性食道炎の患者は世に多くいるため、その症状を素早く、効果的に抑えるテゴプラザンは、患者からの需要が高い薬と予想されます。
私の行きつけの美容院の美容師さんも過去に逆流性食道炎を患ったことがあり、テゴプラザンの話をしましたら、
「逆流性食道炎の症状が出たときは、1秒でも早くすぐに治って欲しいと思った。すぐに治ることが患者からはすごく求められる。」
というようなことを述べていましたので、逆流性食道炎の患者からは、すぐに効果が出るテゴプラザンが求められていると考えられます。
米国の臨床試験結果
テゴプラザンの米国の臨床試験の第III相の結果を説明します。
2025年8月時点で発表されているトップラインデータのみ記載します。
詳細データは、今後、学術誌や学会などで発表されると思います。
記載するといっても、ラクオリアが公開したスライド資料を貼ります。
引用:2025年12月期(第18期)第2四半期(中間期)決算説明会資料
上記のスライド資料は、1枚のスライド内に情報量が多いので、もうちょっと整理して記載しようと思いましたが、まだトップラインデータであり、詳細な情報が出ておらず、維持療法の結果のプレスリリースの文章を読んだだけでは、解釈の仕方がわかりづらい所もあり、間違った解釈で記載するといけないので、会社発表スライドをそのまま貼る形にしました。
ちなみに、臨床試験結果のプレスリリースは以下の2つです。
- EEとNERDの結果について
- EEの維持療法の結果について
ラクオリアの須藤社長がこの臨床試験の結果を受けて、説明会で「快挙」、「大勝利」と述べています。
また、テゴプラザンの米国の導出先の「Sebela Pharmaceuticals」のCEOは、以下のように述べています。
私たちは 40 年以上にわたり、消化器病領域と消化器疾患に苦しむ患者さんのために尽⼒してきました。
テゴプラザンは、従来の PPI 療法では⼗分にコントロールされていない患者さんが持つ⼤きなアンメットニーズに応え、GERD で苦しむ⼈々にとって画期的な新しい治療選択肢となるでしょう。
これらの試験結果は、tegoprazan が GERD の長期管理を再定義する可能性を強く示しています。
より困難な重症例を含むびらん性胃食道逆流症の全範囲にわたって、tegoprazan がすぐれた寛解維持効果を示すだけでなく、既存の治療法と同等の安全性プロファイルを維持しながら胸やけの持続的なコントロールを可能にする点に私たちは大きな期待を寄せています。
当社は、GERD に悩む患者さんのニーズによりよく応えるため、米国での tegoprazan の展開をさらに推進していく所存です。
ワイルコーネル医科⼤学臨床医学教授で、ジェイ・モナハン消化器病センター所⻑のフェリーチェ・シュノール・サスマン医学博⼠は、以下のように述べています。
びらん性胃⾷道逆流症に対するテゴプラザンのデータは、P-CAB が PPI を凌駕する可能性を⽰しており、テゴプラザンが他の薬剤よりも優れている可能性を⽰唆しています。
カンザス⼤学医学部教授で、⽶国消化器内視鏡学会の現会⻑であるプラティーク・シャルマ医学博⼠は、以下のように述べています。
胸やけと胃酸逆流はどちらも GERD の代表的な症状ですが、私たちは通常、胸やけの解消についてのみ議論します。
おそらく、これまでの医学研究では、テゴプラザンのように胃酸逆流の減少を測定して証明することができなかったためでしょう。
(上記の文章の意図の補足説明:NERDにおいて、従来の薬では、胸やけに効くことはあっても、胃酸逆流に効くことはあまりなかったため、今までNERDでは胃酸逆流の解消についてはあまり語られてこなかったけど、テゴプラザンは胃酸逆流を減少させることができるため、今後はその議論もできるようになるというような意味です。)
ワシントン大学医学部教授で神経消化器病学・運動機能プログラムディレクターのプラカシュ・ギャワリマ医学博士は、以下のように述べています。
これらの維持療法のデータは、tegoprazan が、びらん性胃食道逆流症の最も重症な分類においてさえも、持続的な臨床的な意義を持つことを示しています。
これらの結果は全体として、 tegoprazan が治癒と症状緩和を通じて GERD 患者の生活の質を改善するために重要かつ新たな治療選択肢となる可能性を支持するものです。
以上のように、ラクオリアの社長や導出先の企業のCEO、大学の教授らがテゴプラザンの米国の臨床試験結果をベタ褒め、称賛しています。
なぜ、ここまで称賛されているのかというと、その大きな1つが、
テゴプラザンが、先程のGERDの説明で述べた、LA分類のA~Dのグレードを含んだ患者全体に対して、既存薬のPPIであるランソプラゾールより完全治癒の優越性があったということです。
優越性とは、既存薬よりも効果が優れているということであり、統計分析で有意な差があったということです。
ちなみに、この比較対象となった「ランソプラゾール」の商品名が「タケプロン」です。
この何がすごいかと言うと、従来のPPI薬でも、逆流症性食道炎がある程度は治り、臨床試験をする際に既存薬との差が出づらいため、非劣性試験というものを行います。
非劣性試験は、比較する薬と効果が劣っていないことを確かめる試験です。
既存薬と比較して、他に色々メリットがあれば(例えば、すぐに効くなど)、非劣性試験だけでも承認申請できて、薬として販売できます。
今回のテゴプラザンの臨床試験も主要評価項目として、逆流性食道炎の方の試験では、非劣性試験を行いました。
主要評価項目とは、メインに評価する項目であり、それが薬の承認判断の主要根拠となるものです。
そして、それに加えて、副次的評価項目(薬の効果や特徴を補足的に評価する項目)として、優越性の確認も行いました。
つまり、非劣性試験でPPI薬と劣っていないという結果が出れば、それだけでも十分なのですが、優越性も確認したら、まさかのまさかPPIよりも優越性があるという結果が出たのです。
今回の臨床試験の副次的評価項目の内容を見るとLA分類の「グレードA・Bを除いたグレードC・D」の患者の完全治癒の優越性だけを確認する項目もあります。
なぜ、そのような項目を設けたのか会社から公式発表はありませんが、以下のようなことが考えられます。
- 韓国の臨床試験で、重症度が高いグレードC・Dでは、PPIと比較して効果が出やすい傾向というデータが出ていた
- タケキャブの米国の臨床試験でも同様にグレードC・Dの優越性を確認していた
- 薬の承認をする米国FDAは審査等が厳しいので、スムーズに承認してもらうために、既存薬のPPIとの効果の差を明確にしたかった
- 販売後のマーケティングを考慮
そのため、グレードC・Dについては、今回のテゴプラザンの臨床試験において、優越性が出ると最初から予想した上で臨床試験を実施したと思われます。
その結果、グレードC・Dにおいて優越性がありました。
つまり、逆流性食道炎の重度の患者において、既存薬のPPIのランソプラゾールより効くということになります。
ちなみに、競合薬となるP-CABのタケキャブもグレードC・Dについては、優越性がある結果になっています。
そのため、ここまでは、ラクオリアや導出先企業も予想していたのではと思います。
しかし、「グレードC・Dだけを抽出した患者群」ではなく、「A~Dのグレードを含んだ患者全体」でも有意差が出るかどうかは、会社側はやってみないとわからないという予想だったのではと私は推測しています。
少なくとも私は有意差が出るかどうかは、五分五分くらいと予想していました。
だから、「A~Dのグレードを含んだ患者全体」でも優越性があるという結果になったことで、関係者や大学の教授などが驚いて、絶賛しているのではと思います。
ちなみに、タケキャブの米国の承認申請のために行われた逆流性食道炎の臨床試験第III相の結果は以下です。
Efficacy and Safety of Vonoprazan Compared to Lansoprazole in Participants With Erosive Esophagitis
テゴプラザンの評価項目にあった「8週⽬までに完全治癒した全ての患者の割合」については、非劣性試験しがやっておらず、優越性の結果はありません。
また、「2週⽬までに完全治癒した全ての患者の割合」の優越性の試験の結果が載っており、有意差が出ていますが、
「Observed p-value and not a formal test per the preplanned fixed-sequence testing procedure.」
と説明が書かれており、事前に計画された固定順序検定に従った正式な検定ではないです。
そのため、あくまで参考値であり、統計分析の観点から学術的/医学的には信頼性が低い分析結果と考えられます。
そのためか、米国でタケキャブの臨床試験をしていたPhathomの上記の結果の以下のプレスリリースの最初の箇条書きの所にも、全患者群に対する非劣性については記載がありますが、優越性についての記載がありません。
なお、プレスリリースの本文の方には、以下のように、「2週⽬までに完全治癒した全ての患者の割合」と思われる評価項目の記載がありますが、「nominally significant(名目上有意)」と記載があり、統計学的に保証された有意差とは言えない扱いとなっています(「思われる評価項目」と書いた理由は、「ClinicalTrials.gov」と「プレスリリース」に記載のp値が異なっているように見えて、よくわからなかったからです)。
In additional secondary endpoint superiority comparisons, vonoprazan 20 mg healing rates were numerically greater than lansoprazole 30 mg in all patients at Week 2 (p=0.0174)3 and in moderate-to-severe patients2 by Week 8 (p<0.0001) although deemed nominally significant due to the sequential testing method.
さらに、もう1つすごいことは、NERDの臨床試験において、テゴプラザンはプラセボと比較して、「胸やけ」と「胃酸逆流」の両方を改善したことです。
タケキャブの米国の承認申請のために行われたNERDの臨床試験では、「胸やけ」の評価項目があり、そちらは有意差が出ていますが、「胃酸逆流」についての評価項目がありません。
- A Study to Evaluate the Efficacy and Safety of Vonoprazan Compared to Placebo for Relief of Heartburn in Participants With Symptomatic Non-Erosive Gastroesophageal Reflux Disease (NERD)
- Phathom Pharmaceuticals Announces Positive Topline Results from Phase 3 PHALCON-NERD-301 Trial Evaluating Daily Dosing of Vonoprazan for Symptomatic Non-Erosive Gastroesophageal Reflux Disease (NERD)
従来のPPI薬のNERDにおける臨床試験結果は、私は調べていないので、わかりません。
色々書きましたが、述べたかったことは、
「2週目・8週目までに逆流性食道炎の症状が完全治癒した全患者の割合において、テゴプラザンがP-CABのタケキャブも含めた既存薬の中で1番優れている可能性がある」
「NERDの症状において、テゴプラザンは、“胸やけ”と“胃酸逆流”の両方を改善できる」
もっと単純かつ大雑把に書くと
「テゴプラザンが逆流性食道炎を含むGERDの治療薬の中で1番効果がある可能性がある」
となったため、すごい結果というわけです。
「可能性」と強調しているのは、タケキャブとテゴプラザンを同じ実験で直接比較したわけではないからです。
また、何の観点で「効果がある」かは、細かい条件によって変わってきたり、米国で臨床試験をしたことがない他の類似薬の結果はわからないので、あくまで「可能性」と書いています。
ただし、2025年8月時点においては、上記のように推測することが自然だと思います。
ちなみに、テゴプラザンは、韓国と米国のどちらの臨床試験でもNERDにおいてプラセボとの比較で有意差が出ています。
タケキャブも米国ではNERDでプラセボとの比較で「胸やけ」においては有意差が出ていますが、日本では、2回臨床試験をして、2回とも有意差が出ない結果となりました。
そのため、2025年8月現在、タケキャブは、日本でNERDの適応症は実はありません。
しかし、Xのポストなどを見ていると、適応症がないのに、NERD患者においても保険適用でタケキャブが処方されているように見えます。
日本はそこら辺が緩いっぽいです(本当はいけないことです)。
そのため、臨床試験結果の観点では、日本のNERD患者には、タケキャブは効かないということになります。
その他の効果
今回の米国の臨床試験の結果とは関係ないですが、テゴプラザンは、他にも色々メリットがあります。
先述しましたが、テゴプラザンは即効性があり、30分以内~1時間以内で効きます。
GERDの患者は、夜寝る時に胃酸が逆流して、なかなか寝られないことがあります。
例えば、タケキャブでも効くまでに数時間掛かるため、寝るまでに効果が出ずに、しばらく寝られない人もいます。
すぐに効くことは、日中の生活時も大きなメリットですが、テゴプラザンは、寝る頃までには効いてくれるため、生活の質を大きく上げることができます。
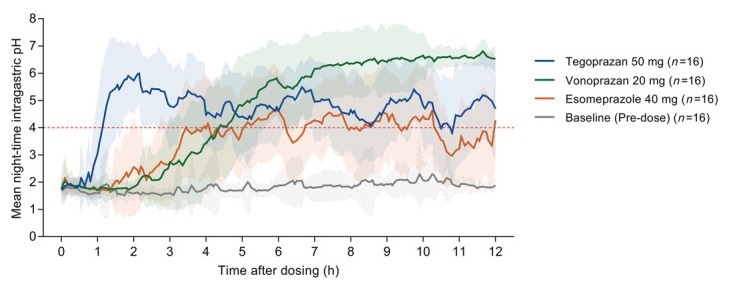
例えば、以下の論文のグラフがわかりやすいです。
Night‐time gastric acid suppression by tegoprazan compared to vonoprazan or esomeprazole
上記の青色の部分がテゴプラザンですが、線がすぐに急激に上がっていて、すぐに効いていることがわかります。
緑色の部分がタケキャブ(Vonoprazan)であり、グラフが上がるまでに時間が掛かっていることがわかります。
他にもテゴプラザンは、腸管バリア機能を改善することで大腸炎を予防するという論文もあります。
さらに他にもテゴプラザンは、色々なメリットがあり、論文等があるのですが、論文の量が多くて、ここでは紹介しきれません。
テゴプラザンは、逆流性食道炎などのGERDに速く効き、よく効き、既存薬と比較して他にも色々メリットがある薬です。
安全性
テゴプラザンは、既に韓国や中国、その他のいくつかの国で使われている薬です。
臨床試験の結果では、安全性および忍容性は、プラセボおよびランソプラゾールと同程度であり、既存薬のPPIと比較して安全性の問題は出ていません。
テゴプラザンは、薬物相互作用が低いという特性もあります。
薬物相互作用とは、複数の薬を同時に使用した際に、予期しない副作用が発生したりする現象のことです。
つまり、薬物相互作用が低いほど、他の薬との併用時に安全性が高いということです。
薬物相互作用関連の研究の1つとして、以下の記事がHKイノエンから発表されています。
経皮的冠動脈形成術(PCI)を受けた急性心筋梗塞(AMI)患者のうち、二重抗血小板療法(DAPT)とともに、PPI系薬物またはテゴプラザンを服用した患者を比較しました。
その結果、テゴプラザン服用群は、1年内の消化管出血リスクがPPI服用群に比べ約28%低いことが示され、心筋梗塞や脳卒中などの主要心脳血管イベント(MACCE)のリスクが増加しないことが確認されたとのことです。
従来のPPI薬と比較し、薬物相互作用が低いこともテゴプラザンのメリットです。
タケキャブは、米国での承認申請の審査中に、発がん性が懸念されている「ニトロソアミン不純物」が検出され、その対応で承認まで長引いていました(今は管理体制が整えられて問題ないです)。
FDA’s Decision on Vonoprazan Delayed Due to Nitrosamine Impurity
一方、テゴプラザンは、以下の韓国記事によると、そもそも化合物構造上、ニトロソアミン不純物が検出される可能性が低いそうです。
FDA 통과 못한 ‘다케켑’…HK이노엔 ‘케이캡’ 반사이익 얻을까
また、タケキャブは、PPIと比較してガストリン値が高くなりやすいです。
以下の記事にそのことについて記載されています。
テゴプラザンもガストリン値が上がりますが、GERDの治療時はPPIと同程度です。
ただし、興味深いことに、GERDの維持療法として半量のテゴプラザン 25mgと半量のランソプラゾール 15mgを維持療法中の24週間投与の間で比較した結果、テゴプラザンの方が血清ガストリン値が有意に低く維持され、高ガストリン血症の発症の割合も有意に低かったという研究があります。
ガストリン値が高い状態が続くと色々な病気を引き起こす可能性があります。
ただし、薬を飲まないと結局、他の病気になったり、生活に支障をきたすので、このくらいの副作用なら、GERDの症状がある人は飲んだ方が健康面で良いと言われています。
ちなみに、アルコールなど他の飲食物でもガストリン値が上がるものがあります。
GERD以外の他の薬も色々な副作用があります。
そのため、メリット・デメリットを考えて、どこまで細かく気にするかです。
ちなみに、タケキャブのガストリン値の高い上昇について、問題ないと主張する人もいますが、悪魔の証明(色々な要因を排除した上で、追跡調査する必要があり、その調査が困難なので証明が難しい)なので、本当に問題ないかはわかりません。
とは言っても、従来のPPIもテゴプラザンもタケキャブも無理矢理、酸を抑制しているものなので、不必要な投与、長期服用は避けた方が良いでしょう(逆流性食道炎の薬に限らない話)。
逆流性食道炎の治療には、「オンデマンド療法(症状が出そう、出たときに薬を使用し、症状が消えたら薬の使用を中止する)」というのもありますが、テゴプラザンの場合は、投与後にすぐに効くため、オンデマンド療法に適している可能性があります。
自称薬剤師に上から目線で批判された過去
まだテゴプラザンが韓国でのみ臨床試験が完了して、米国での開発が決まっていなかったときに、X(旧Twitter)上で、私がテゴプラザンの米国進出について期待するポストをしました。
そのときに、自称薬剤師の全く知らないアカウントの人から、
「テゴプラザンは米国で開発、販売されることはない」
「従来の薬で事足りる」
というようなリプライをされ、超超超上から目線で批判されました。
その頃からX上の自称薬剤師は、傲慢なうんこが多いと私が思うようになったのはさて置き(その後にも、おそらく異なる自称薬剤師からも、逆流性食道炎の新薬なんて必要ないと批判された)、その薬剤師を見返して、米国でも発売して欲しいと思っていました。
そして、時が過ぎ、米国での開発が決まり、臨床試験が行われ、ついに、臨床試験完了まで来ました。
しかも、既存薬と比較し、素晴らしい臨床試験の結果を出しました。
あとは、米国FDAに承認申請を出し、順調にいけば、2026年末~2027年の初め頃に発売される予想となっています。
こんな良いデータを出したテゴプラザンは、逆流性食道炎の患者を含む、多くのGERD患者の症状を改善し、多くの人々の生活を豊かにすると思われます。
そもそも、テゴプラザンは開発の最初の頃から「すぐに効く」ということがわかっていたので、その「すぐに効く薬」をこの世に必要ないと断言する薬剤師は、まったく患者のことを考えていません。
患者のことをまったく考えない、自分のことしか考えず、患者を見ずに自分の考えですべて物事を決めるクソ野郎です。
クソ薬剤師です。
(言葉が悪いのはご了承ください)
逆流性食道炎の症状をすぐに緩和させることは、多くの患者が求めていることだと思います。
実際に、私の行きつけの美容院の美容師さんもそれを求めていました。また、X上のポストを見てもそれを求めている患者がいます。
それを求めている多くの患者を無視して、必要ないと言うのは、
「人の心とかないんか?」(呪術廻戦、禪院直哉風)
と思います。
それでよく薬剤師の仕事をしているなと思います。
米国で開発開始された時点で自称薬剤師の予想はハズれていますが、もうここまで来たら発売はされるとは思いますので、米国で販売されないという薬剤師の予想がハズれ、私の予想が当たったということになります。
薬の専門家より専門外の素人の私の方が、薬の行方の予想が当たりました。
X上の自称専門家の話は当てにならないということがわかりました。
私はIT関係の仕事をしていますが、X上のITエンジニアのアカウントもよく間違っていることをポストしているので、X上の自称専門家の話は、あまり信用しない方が良いかもです。
「そうではないと思う」と軽い主張をするくらいだったらまだしも、「私は専門家だ。お前はど素人だから、何もわかっていない!」という感じで、超高圧的に批判してくることが非常に厄介です。
ちなみに、その批判をしてきた自称薬剤師の人だったと思いますが、なぜか武田薬品のことは、べた褒めしていて、「お前ら下々共は武田薬品の能力を舐めるな」みたいな感じでも批判してきたので、もしかすると武田薬品のファンであり、タケキャブの競合薬となるテゴプラザンやそれを創出したラクオリアを否定したかったのかもしれません。
何はともあれ、このままいけばテゴプラザンが米国で販売され、多くの患者の生活の質(QOL)を上げることになるであろうことは、とても喜ばしいことです。
患者が何を求めているのか、患者のことを考えられる医療関係者が増えて欲しいと願いします。
(補足:すべての薬剤師が傲慢というわけではありません。X上の一部の薬剤師のみの話です。)
日本での開発・販売状況
2025年8月時点で、テゴプラザンは日本での開発は止まっています(臨床試験が行われていない)。
実は、過去に日本で臨床試験第I相は行われています。
その後、韓国企業のHKイノエンにテゴプラザンを導出し(権利を渡し)、主に韓国で優先して開発が行われていました。
テゴプラザンは、既に多くの国々で販売、開発されているのに、なぜ日本では開発が止まったままなのでしょうか?
その主な原因は、日本の薬価政策です。
何年か前から日本の自民党や厚労省などは、日本の薬の薬価(保険適用の処方薬の価格)を低くするように推し進めています。
その理由は、少子高齢化もあり、医療費を使う高齢者や生活保護者が増え、社会保障費が莫大になっているからです。
そのため、社会保障費を減らすために、薬価を減らしているわけです。
薬を1つ作って、販売し、患者の手元に届くまでには、以下のように莫大なお金が掛かります。
- 1つの薬を生み出すのに、研究開発費で何百億円~数千億円掛かる
- 薬を製造するのに、原材料費や製造管理費などが色々掛かる
- 薬を販売するのに、管理費やマーケティング費用などが色々掛かる
このように薬1つを患者に届けるまでに莫大な費用が掛かっています。
このような状況下で、薬価を下げるとどうなるかというと、製造するだけでも製造費用で赤字になり、採算が取れなくなります。
また、必ず臨床試験が成功するわけでもないので、失敗リスクを考慮し、色々な薬を作り出すことを考えたら、1つの薬の開発費だけではなく、他の薬の開発費も一部賄えるくらいの利益が販売後に出ないと採算が合いません。
今は、物価高(インフレ)になっていますので、なおさら製造費などが上がり、薬価が低いと赤字になりやすくなっています。
逆流性食道炎の薬は、がんの治療薬などとは異なり、薬価が非常に低いです(患者からしたらそれでも高いと思うかもしれませんが)。
そのため、日本政府による低薬価政策によって、採算が合うか不透明になり、その結果、テゴプランの開発が止まっています。
「ドラッグ・ロス」、「ドラッグ・ラグ」が実際に起こってしまっている状況です。
最近では、このような話がジェネリック医薬品であり、採算が取れなく、販売が終わるジェネリック医薬品が出てきていて話題になっていますが、新薬ですらこれが起こっている状況なのです。
しかも、海外の創薬企業・製薬企業の薬ではなく、日本の創薬バイオベンチャー企業が創出した薬でドラッグ・ロスが起こっています。
日本の低薬価政策によって、日本企業が創出した薬が、海外では販売でき、日本では販売できない状況になっているのです(2025年8月時点の話)。
最近、日本政府は、日本の創薬産業を成長させようと「創薬力」などと謳って、創薬関係に力を入れています。
その一方、日本の創薬バイオベンチャー企業が創出した素晴らしい薬を日本で販売することを困難にする政策をしていて、本末転倒な状況です。
日本政府は、日本の患者のためにもならない、日本の創薬企業育成にもならない矛盾したことをやっていることになります。
本日2回目の「人の心とかないんか?」(呪術廻戦、禪院直哉風)です。
また、テゴプラザンは、「すぐに効き、よく効き、安全性もある」薬ですので、既存薬を使うよりテゴプラザンを使った方が患者の健康は良くなりやすい可能性があります。
もしその場合は、患者はテゴプラザンによって健康を保ちやすくなり、既存薬を使うよりも長期的に見たら、病院に行くことも減り、医療費、社会保障費が削減される可能性があります。
つまり、日本政府がこの薬価政策を改善しない限り、日本人は効果が低い薬を使い続け、健康もそこまで良くならず、労働力や経済活動が低下し、社会保障費も増大させ、税金もアップするという負のスパイラルに陥る可能性があるわけです。
もうわけがわからない、日本はどこに突き進んでいるの?状態です。
そのような経緯がありますが、ラクオリアはそれでも患者のためにがんばっており、色々工夫してコストを抑えるなど努力して、日本で開発・販売できるようにしている最中です。
ラクオリアの過去の説明会において社長が、
「日本の会社である以上日本の患者さんに届けることが重要な使命」
「進行するドラッグロスを目の前にしてそれに加担してよいのか」
と述べ、ラクオリアが日本の患者のために一生懸命にがんばっています。
さすがに、米国の臨床試験でこんなに素晴らしいデータを出し、逆流性食道炎の多くの患者を苦痛から救い、生活の質を大きく上げられる薬を日本で販売できないのは、日本国民の大きな損失になります。
しかも、自国の企業が創出した薬を自国でだけ販売できないのは、もはやわけわからない状況です。
こんなおかしなことは、絶対にあってはならないことです。
日本国民のため、日本の患者のために、社会的責任がある日本の大手製薬会社や日本政府は、なんとかテゴプラザンを世に届け、多くの患者を救い、幸せを届けるよう尽力してくださると期待しています。
参考:以下のURL先に、テゴプラザンの他国の進出状況などをまとめています(私が書いたもの)。
ラクオリア創薬のテゴプラザンの収益
ラクオリアのビジネスモデルの1つは、ロイヤルティビジネスです。
テゴプラザンもそれであり、テゴプラザンを開発・販売する権利を他社に渡して(導出して)、その開発段階などに応じてマイルストンとしてお金をもらったり、販売されたら売上の一部をロイヤルティとして、導出先からもらっています。
2025年8月現在、日本以外の全世界の権利をHKイノエンに渡しています。
また、HKイノエンは、さらに各国の企業に権利を渡していたりします(サブライセンス)。
以下のURL先に、ビジネスモデル、ロイヤルティについて説明しています(私が書いたもの)。
ラクオリアは、HKイノエンに導出した分のロイヤルティ料率を細かくは発表していませんが、過去の説明会等から予想するに、1桁%台のどこかだと推測します。
そのため、仮にロイヤルティ料率が5%と仮定して、HKイノエンの目標通りテゴプラザンが3000億円売り上げた場合は、
3000億円 × 5% = 150億円
がラクオリアに入ってくることになります。
だいぶ入ってくるお金が減りますが、自分たちで製造や販売をしないので、基本的にそういった費用が発生しません。
そのため、ロイヤルティとして受け取ったお金の多くを粗利にしやすくなります。
ちなみに、ラクオリアが自社で日本の開発を最後までして、自社販売すれば良いのでは?と考える方もいると思いますが、日本で逆流性食道炎の新薬の臨床試験の第III相をするだけでも、通常で数百億円掛かってきます。
また、製造などの設備投資や人員を揃えるのも大変です。
小さいバイオベンチャー企業では、そこまでの体力がないため、今回の薬においては、大企業に導出することが基本戦略になります。
もし、大手ファンドに何百億円、何千億円の先行投資をしてもらうことができたら、自社や新会社を設立して開発することもできるかもしれません。
しかし、日本の現在の低薬価政策において、そこまでリスクを取るファンドがいるか怪しく、仮に、そのようなファンドがいたとしても、一から開発や製造などの準備をすることは大変、かつ、時間が掛かるため、その選択肢を取る経営者は少ないと思います。
さいごに
テゴプラザンが米国の臨床試験で大変素晴らしい結果を出しました。
テゴプラザンは、世界の多くの人々を助けることになるでしょう。
日本でも販売され、多くの日本人を救い、幸せをもたらしてくれることを願います。
【宣伝】
LINEスタンプを作りました。
株などの投資全般の会話で使えます。
日常会話でも使えるスタンプとなっています。
ぜひ、使っていただけたら嬉しいです。







コメント